

免洗免灭RTU是指在特定环境(ISO Class 8+ISO Class 5)生产完成的COP西林瓶被放置在托盘或巢盘中进行密封并用袋子包装,控制COP西林瓶的微生物负载和不溶性颗粒,再经过辐照灭菌处理后,可达到...[查看详情]
CDE发布《嵌合抗原受体T细胞治疗药品说明书临床相关信息撰写指导原则》[查看详情]
2026-02-27
在药品包装的世界里,干燥剂的选择常被简化为成本或习惯的考量。然而,对于真正理解药品稳定性核心的研发与质量专家而言,这是一项基于分子层面相互作用的精密科学决策。面对分子筛与硅胶这两种...[查看详情]
2026-02-27CDE发布《罕见病用化学药物药学研究指导原则(试行)》[查看详情]
2026-02-26
在干细胞治疗、细胞培养与再生医学的精密世界里,培养体系的稳定性是决定实验成败与产品质量的基石。其中,生长因子——这些微量的蛋白质信号分子,如同指挥细胞增殖、分化和功能的“交响乐指挥...[查看详情]
2026-02-26CDE发布《碘[131I]化钠口服溶液仿制药药学研究技术要求》[查看详情]
2026-02-25CDE发布治疗间质性肺疾病的抗纤维化药物临床试验技术指导原则(试行)[查看详情]
2026-02-09
传统细胞药物生产线曾面临一个棘手难题:包装西林瓶需要经过复杂的清洗、灭菌、去热原处理,不仅耗时长达数小时,还增加了微生物污染和内毒素超标的双重风险。RTU免洗免灭COP西林瓶的出现,通过...[查看详情]
2026-02-05
随着国家集采的深入推进和药品质量要求的不断提高,已通过或正在申报一致性评价的药品可能会面临防潮包装变更的需求。无论是为了优化成本、提高稳定性还是变更供应商,防潮包装的变更都不能简单...[查看详情]
2026-02-04
COP西林瓶通过其独特的材料特性和精密的设计,为外泌体在超低温环境下的长期稳定储存提供了关键保障。下面这个表格清晰地展示了它的核心保护机制。...[查看详情]
2026-02-03CDE发布细胞治疗药品药学变更研究与评价技术指导原则(试行),随着细胞治疗领域迅猛的技术迭代、工艺的持续优化、迫切的产能扩增需求和原材料及耗材的更新替代,细胞治疗药品在研发和上市后阶...[查看详情]
2026-02-03
2025版《中国药典》在微生物控制方面进行了重要升级,除了你提到的洋葱伯克霍尔德菌群(BCC),还明确并强化了对多种“不可接受微生物”的监控要求。下面这个表格帮你快速了解这些新增的重点监...[查看详情]
2026-02-02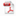
CDE发布《化学药品创新药晶型研究技术指导原则(试行)》的通告[查看详情]
2026-01-29
在药品防潮包装系统中,干燥剂的选择远非简单的成本或惯例决策,而是一项基于严谨科学数据的策略。分子筛与硅胶,作为最常用的两大固态干燥剂,其吸附机理、性能特性和潜在风险存在显著差异。随...[查看详情]
2026-01-29
在COP(环烯烃共聚物)西林瓶的超低温储存过程中,评估外泌体聚集程度是一个多维度的科学过程。这不仅关乎包装材料的选择,更涉及具体的物理和化学检测指标。结合COP材料的特性及外泌体药物的质...[查看详情]
2026-01-28
CDE发布《多糖结合疫苗核磁共振研究的技术考虑(试行)》的通告[查看详情]
2026-01-27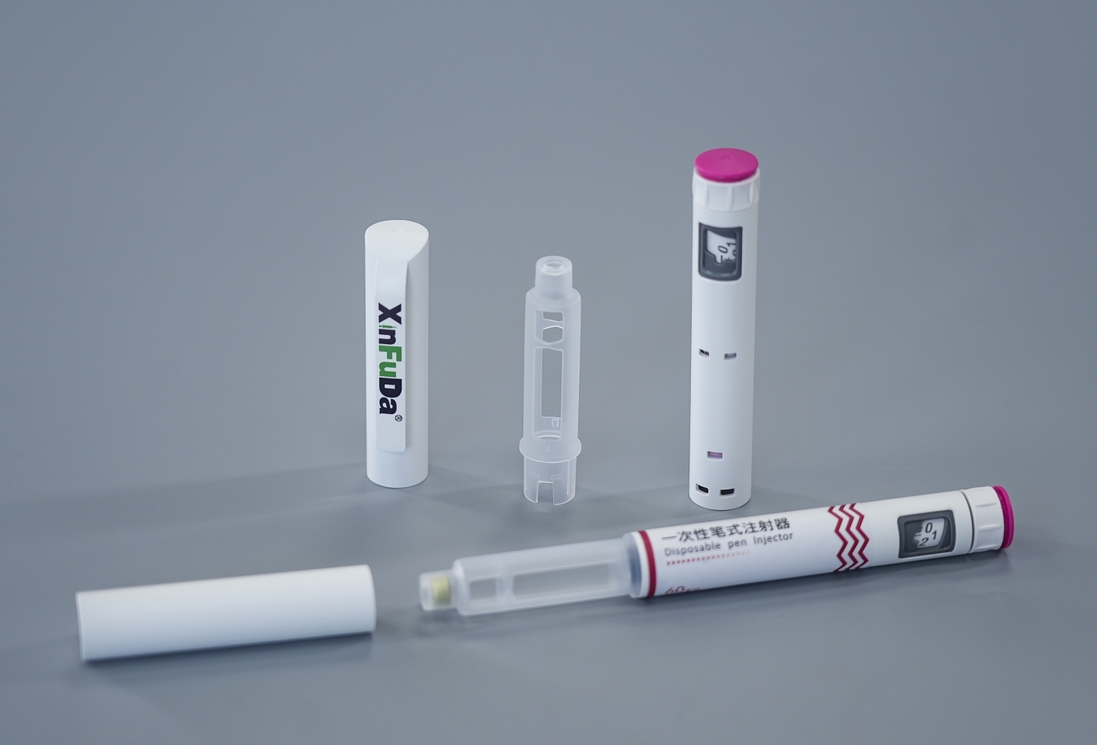
笔式注射器作为一种精密给药系统,其质量控制的严格性不言而喻。每一支注射笔都需经过多项精密测试,确保在临床使用中能够稳定、安全地输送药物。针头连接牢固度和笔帽分离力作为两个关键物理性...[查看详情]
2026-01-27
口服液体药用聚丙烯压旋盖的质量控制是确保药品安全的重要环节。相关的YBB标准(如YBB00092002-2015)进行了一系列更新,对测试方法提出了更严格、更细致的要求。...[查看详情]
2026-01-26CDE发布《局部起效化学仿制药物理化学及结构(Q3)特性研究技术指导原则(征求意见稿)》[查看详情]
2026-01-23
在超低温储存中,COP西林瓶通过其独特的材料特性与科学的工艺设计,能有效减缓外泌体的聚集和沉淀。以下是关键措施和原理的概要。[查看详情]
2026-01-23
口服液体药用聚丙烯压旋盖的性能测试是一个系统性的质量评估过程,核心目标是确保其密封完整性、材料安全性、物理机械性能以及微生物安全性符合药品包装的严格要求。以下是依据相关药包材标准(...[查看详情]
2026-01-22
 冀公网安备 13010802000997号
冀公网安备 13010802000997号 微信扫一扫
微信扫一扫