

免洗免灭RTU是指在特定环境(ISO Class 8+ISO Class 5)生产完成的COP西林瓶被放置在托盘或巢盘中进行密封并用袋子包装,控制COP西林瓶的微生物负载和不溶性颗粒,再经过辐照灭菌处理后,可达到...[查看详情]
随着2026年3月20日司美格鲁肽化合物专利保护期届满,制药行业即将进入新的发展阶段。这一变化不仅影响药物市场格局,更对配套给药装置的技术研发提出了新的要求。...[查看详情]
2026-03-24
外泌体作为天然的纳米级递送载体与疾病调节因子,已成为新一代治疗药物与诊断工具开发的热点。然而,其纳米尺度(30-150 nm)与脆弱的脂质双分子层结构,使得外泌体药物在制备、储存与运输环节...[查看详情]
2026-03-24
在药品稳定性保障体系中,防潮包装是抵御水分侵蚀的关键屏障。然而,包装材料本身与药品的长期接触,可能带来另一重隐忧——可提取物与浸出物。对于内含干燥剂(如硅胶、分子筛)或采用多层复合...[查看详情]
2026-03-19
2025年,中国药品集中采购进入“稳价提质”的新阶段。第十一批国采规则明确转向“防围标、反内卷”,通过设置“锚点价格”和尊重临床品牌选择,引导行业从单纯的价格博弈转向 质量、供应与创新...[查看详情]
2026-03-18
取HDPE瓶数只,加入标示容量1/2的氯化钠注射液,将盖盖紧,振摇1分钟,即得供试液。供试液进行薄膜过滤后,依法检查在(中国药典2015版通则1105微生物计数法、1106控制菌检查法),细菌数每个瓶...[查看详情]
2026-03-17
在再生医学与细胞治疗飞速发展的今天,干细胞库作为保存生命种子的“诺亚方舟”,其核心使命在于长期、安全、高效地储存珍贵的细胞资源。无论是脐带血造血干细胞、间充质干细胞(MSC),还是诱...[查看详情]
2026-03-17
原料药、药用辅料和药包材CDE登记信息查询[查看详情]
2026-03-16CDE发布《流感病毒疫苗临床试验技术指导原则(试行)》的通告[查看详情]
2026-03-13
2026年1月1日新版《中国药典》正式实施,其中新增的 通则9211《非无菌药品微生物控制中水分活度应用指导原则》首次将水分活度(aw)这一关键物理化学参数,确立为药品微生物风险评估的核心科学...[查看详情]
2026-03-12
在生物制药与细胞治疗领域,无菌保证是产品质量不可逾越的生命线。传统的西林瓶无菌处理流程,依赖于一套复杂且资源密集的“厂内清洗、灭菌”体系,而随之而来的“清洗验证”更是压在质量与生产...[查看详情]
2026-03-11
在药品关联审评日益严格的今天,儿童安全盖的功能被精准地一分为二:“儿童难开”的主动防护,与“长期密封”的被动保障。后者,即密封性,是保证药品在从出厂到患者手中的整个生命周期内,不受...[查看详情]
2026-03-10
药品包装系统密封完整性是确保注射剂等无菌药品在其整个生命周期内免受微生物污染、保持内容物稳定的生命线。随着《化学药品注射剂包装系统密封性研究技术指南(试行)》及2025版《中国药典》相...[查看详情]
2026-03-09CDE发布《预防用mRNA疫苗临床试验技术指导原则(征求意见稿)》[查看详情]
2026-03-06
在细胞药物(如CAR-T、干细胞制剂、TIL疗法)的商业化生产竞赛中,“时间”是最昂贵的原材料,而“工时”是其中可量化、可优化的关键成本。 从临床样品的制备到商业化规模的扩大,传统的西林瓶...[查看详情]
2026-03-05
注射笔作为糖尿病、生长激素缺乏症等慢性疾病患者日常给药的关键器械,其质量可靠性直接关系到治疗效果与用药安全。在众多质量控制指标中,针头连接牢固度与笔帽分离力是两个常被忽视却至关重要...[查看详情]
2026-03-05
口服液体药用聚丙烯压旋盖的化学稳定性非常优异,这是其能够作为药品直接接触包装材料的核心基础。这种稳定性源于聚丙烯(PP)材料本身的分子结构特性,并通过严格的药包材标准(如YBB、USP)进...[查看详情]
2026-03-04药典委发布棕氧化铁药用辅料标准草案公示稿[查看详情]
2026-03-04
在药品开发中,原料药的多晶型现象早已不是冷门知识,但其对引湿性的深刻影响,却常被简化为一个“是或否”的吸湿性指标。事实上,不同晶型之间引湿性的差异,足以导致同一配方、同一工艺生产的...[查看详情]
2026-03-03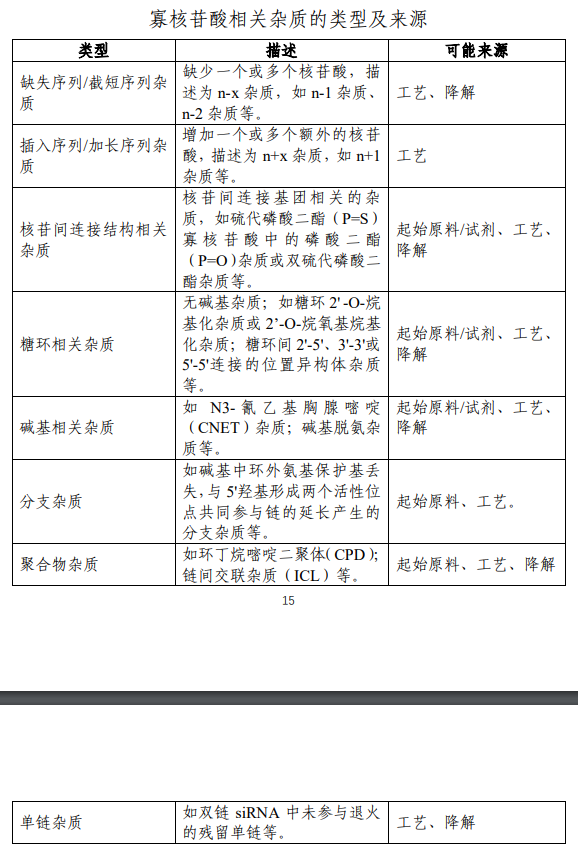
CDE发布《化学合成寡核苷酸药物(创新药)药学研究技术指导原则(试行)》[查看详情]
2026-03-02
2026年1月1日新版《中国药典》正式实施,其中新增的通则0862《元素杂质限度和测定法》标志着我国药品质量控制正式与国际ICH Q3D标准全面接轨。对于口服液等液体制剂企业而言,新规带来的不仅是...[查看详情]
2026-03-02
 冀公网安备 13010802000997号
冀公网安备 13010802000997号 微信扫一扫
微信扫一扫